传统紫杉醇是目前临床治疗乳腺癌、非小细胞肺癌、卵巢癌等多种肿瘤的最有效药物之一, 亦是涵盖多种肿瘤的广谱化疗药物。在早期研发中,因紫杉醇难溶于水, 所以紫杉醇注射液是以聚氧乙基代蓖麻油和无水乙醇组成混合溶媒制成的注射剂, 为预防因上述溶媒引发的过敏反应及超过敏反应, 临床上普遍采用大剂量激素加组织胺受体拮抗剂作为紫杉醇注射液使用前的常规预处理, 即便如此,仍然无法杜绝过敏反应和超过敏反应的发生。此外, 因使用预处理方案, 限制了伴有严重糖尿病、高血压和胃溃疡等基础病变的肿瘤患者使用。
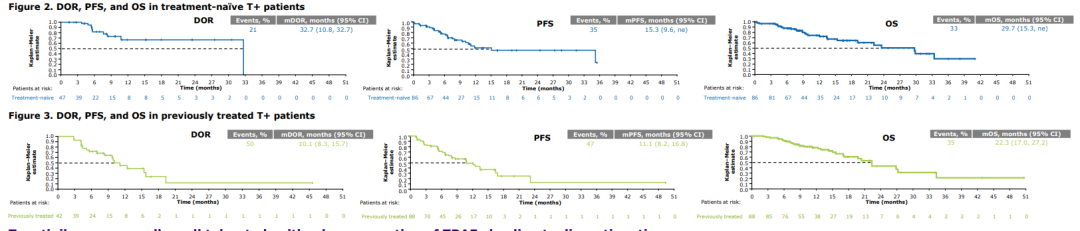
目前在紫杉醇基础上有两种改良型新药,其一是注射用紫杉醇脂质体,该药是以磷脂、胆固醇等为膜材料, 采用特殊制备工艺将紫杉醇包裹在脂质体中, 不再使用混合溶媒, 避免了因使用混合溶媒而对人体所产生的毒副反应。一项纳入14 个随机对照试验(RCT),包括980例患者的Meta分析结果显示[1],紫杉醇脂质体联合顺铂在治疗晚期非小细胞肺癌患者所导致的恶心、呕吐、肌肉、四肢痛、周围神经炎以及过敏反应如皮疹和呼吸困难等不良反应发生率方面明显低于普通紫杉醇联合顺铂,且其疾病控制率(DCR)优于普通紫杉醇组(82.2% vs. 75.5%, P<0.05)。
由于脂质体的结构特性,紫杉醇脂质体给药后易被单核-巨噬细胞系统识别并吞噬,集中于网状内皮系统发达的器官,淋巴结正是其中之一。淋巴结转移是肿瘤的重要转移途径,其转移数量与预后负相关[2,3]。紫杉醇脂质体相对传统紫杉醇注射液在淋巴结分布浓度更高,或可能具有更强的抗肿瘤淋巴结转移作用,对此,值得从机制和临床角度进行深入研究。一项对比紫杉醇脂质体联合顺铂方案(LP)与吉西他滨联合顺铂方案(GP)一线治疗Ⅲ/Ⅳ 期肺鳞癌的临床研究[4]显示紫杉醇脂质体能显著抑制区域淋巴结转移,使患者获得更高的无进展生存(PFS)。

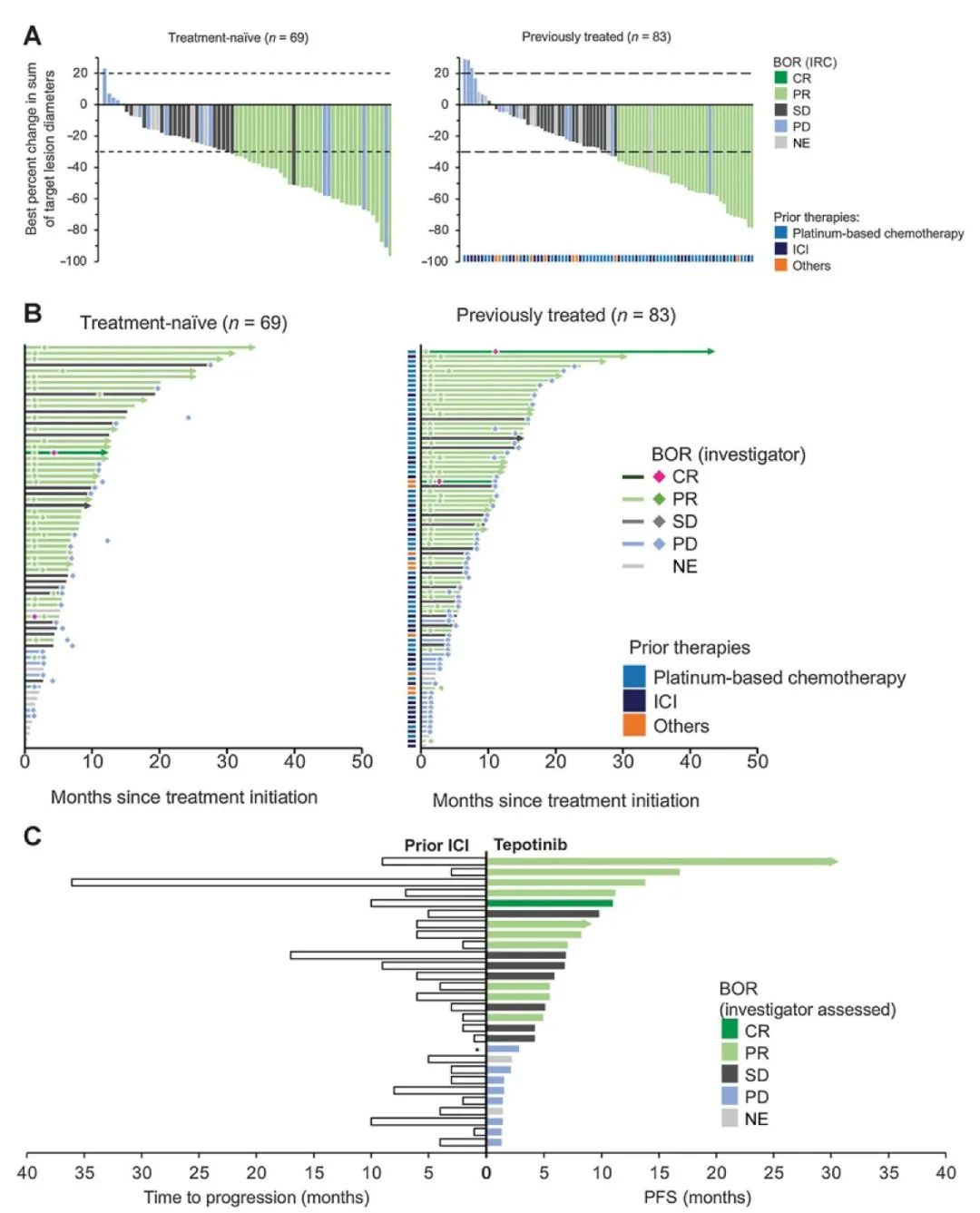
白蛋白结合型紫杉醇是目前广受关注的新型紫杉醇类药物,采用纳米技术,借助天然白蛋白增加紫杉醇的药物递送和生物利用度,同时避免了有机溶剂引起的超敏/毒性反应,不需要激素预处理。与溶剂型紫杉醇比,白蛋白紫杉醇具有使用方便的特点。美国FDA已批准白蛋白紫杉醇应用于乳腺癌、非小细胞肺癌等瘤种。在中国目前正式批准的适应证尚只有乳腺癌。
全球Ⅲ期研究CA031对比每周白蛋白结合型紫杉醇联合卡铂和溶剂型紫杉醇加卡铂一线治疗晚期非小细胞肺癌的结果显示:前者可显著改善晚期肺鳞癌患者的客观缓解率(ORR,41% vs. 24%),但遗憾的是白蛋白结合型紫杉醇ORR的优势并未转化为生存时间的受益[5]。安全性方面,白蛋白紫杉醇的神经毒性、中性粒细胞减少和关节疼痛发生率更低,而紫杉醇组血小板减少和贫血发生率更低。
图3.CA031生存期对比
在免疫治疗如火如荼发展的今天,紫杉醇类药物与免疫联合进行了多瘤种的探索。紫杉类药物通过稳定微管蛋白抑制细胞分裂起作用,同时具有脂多糖模拟物作用,可以激发巨噬细胞介导的肿瘤细胞杀伤作用。此外,紫杉类药物还是较强的免疫活化剂,可以激活CD8+T细胞,降低免疫抑制细胞,如调节性T细胞作用。紫杉类药物可以调节免疫系统的多个功能,包括招募淋巴细胞、促进免疫增强的细胞因子释放,如IL-12、IFNΥ、TNFα和GMCSF,这些都有可能增加免疫治疗的抗肿瘤活性。
以晚期肺鳞癌为例,KEYNOTE-407研究[6]对比了帕博利珠单抗联合卡铂+紫杉醇或白蛋白紫杉醇和单纯化疗一线治疗晚期肺鳞癌,接受紫杉醇或白蛋白紫杉醇化疗的患者基线特征均衡。结果未观察到不同化疗方案的总生存(OS)有差异,无论患者选择紫杉醇卡铂或白蛋白紫杉醇卡铂,帕博利珠单抗联合化疗均可以改善患者的OS。其中,帕博利珠单抗联合紫杉醇卡铂对比单纯化疗的中位OS分别为14.0个月vs10.3个月,HR =0.67(0.48-0.93);帕博利珠单抗联合白蛋白紫杉醇卡铂对比单纯化疗的中位OS分别为NR vs 12.6个月,HR=0.59(0.36-0.98)。
联合治疗组疗效获益亦较明显。帕博利珠单抗联合紫杉醇卡铂或白蛋白紫杉醇相较单纯化疗的ORR分别为57.4% vs 37.7%及58.7% vs 39.5%。
发表在JCO的一项回顾性研究显示,激素类药物的使用可能影响免疫治疗疗效,但在KEYNOTE-407研究中,为预防恶心,患者在接受紫杉醇或白蛋白紫杉醇治疗前均常规使用预防性激素类药物治疗,两组总体的激素使用量相似,未观察到类固醇使用对免疫治疗疗效的影响。对此,需要更多的研究证实。
在精准医学时代,化疗依然是抗肿瘤治疗的基石。不同治疗方式的有机结合,包括靶向治疗、免疫治疗与化疗、放疗甚至手术的结合,以及多学科协作,必将改善肿瘤的生存,增加其治愈可能,给肿瘤诊治带来更为明媚的春天。